近日,安徽大学信息材料与智能感知安徽省实验室吴李君教授团队与合肥工业大学合作,利用分子内加速组装分子信标,开发了一种基于三维DNA纳米结构空间限制效应的信号放大方法,用于快速、高效、可靠地检测末端脱氧核苷酸转移酶的活性。相关成果以“Intramolecular Accelerated Assembly of Molecular Beacons: a DNA Nanoarchitecture-based Spatial Confinement Strategy Toward Terminal Deoxynucleotidyl Transferase Biosensing”为题发表于国际权威学术期刊《Analytical Chemistry》(DOI: 10.1021/acs.analchem.3c03103)。安徽大学为第一完成单位,博士研究生王旗为论文第一作者,吴李君教授与合工大徐建国教授为论文共同通讯作者。
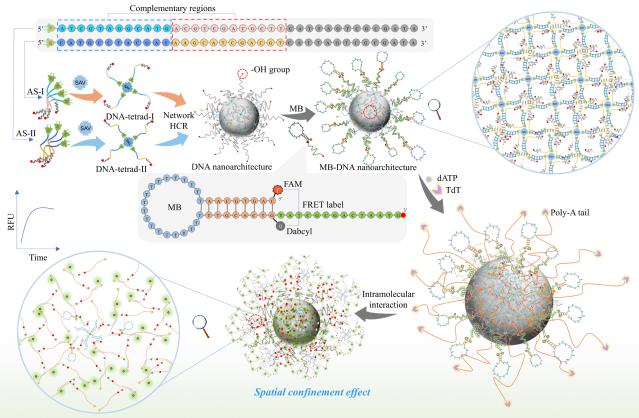
末端脱氧核苷酸转移酶(TdT)在临床医学和血液病理学中的生理功能分析凸显了其作为一种诊断性生物标志物在急性白血病诊断中的实际应用意义。该研究设计了一种分子内加速组装的分子信标(MB),利用三维DNA纳米结构的空间限制效应,实现了对TdT活性的快速实时分析。在该方法中,三维DNA纳米结构通过交联网络杂交链反应(HCR)构建而成,偶联在支架DNA纳米结构上的MB含有大量游离的羟基(-OH)末端,当TdT存在时,游离的-OH基团可以立即被TdT识别并通过分子内加速组装过程与许多MB快速反应,MB的荧光强度可以随时间变化显著增强,从而稳定地分析TdT活性。
研究结果表明,基于DNA纳米结构的空间约束效应使得高分子碰撞频率加速了反应动力学,即使在20分钟内,该方法也具有很高的灵敏度。此外,基于DNA纳米结构的检测方法在从人血清中筛选TdT方面表现出良好的生物稳定性,这预示着在进一步监测活细胞中TdT方面具有极大的潜力。本项工作为解决TdT分析中低反应动力学和效率的局限性提供了新的见解,而且为相关疾病诊断奠定了研究基础。此外,该方法还可以扩展到其他重要的临床生物标志物的检测,实际应用潜力巨大。
新闻链接:http://www.ahu.edu.cn/2023/0829/c15059a313840/page.htm
网站内容来源于互联网,由网络编辑负责审查,目的在于传递信息,提供专业服务,不代表本网站平台赞同其观点和对其真实性负责。如因内容、版权问题存在异议的,请与我们取得联系,我们将协调给予处理(按照法规支付稿费或删除),联系方式:ahos@aiofm.ac.cn 。网站平台将加强监控与审核,一旦发现违反规定的内容,按国家法规处理,处理时间不超过24小时。